製薬会社などに設けられている「ファーマコビジランス(PV)」とは、どんな職業なのでしょうか?
具体的な職責・仕事内容や求められるスキル、就職先、平均年収、一日のスケジュール、業界トレンドとともに、未経験者でも可能なのか、転職成功のコツについてもお伝えします。
目次
ファーマコビジランス(PV)とは?
ファーマコビジランスの仕事内容
ファーマコビジランスの就職先
ファーマコビジランスの一日のスケジュール
ファーマコビジランスに求められるスキル・資格
ファーマコビジランスは未経験でも可能か?
ファーマコビジランスの平均年収
ファーマコビジランスが把握しておきたい業界トレンド
ファーマコビジランスに関するよくある質問(Q&A)
ファーマコビジランスへの転職を成功させるためには
ファーマコビジランス(PV)とは?
「ファーマコビジランス」とは、英語でいうPharmacovigilance(Pharmaco=薬のvigilance=監視)(略してPV)のことで、「医薬品の安全性監視」という意味です。
製薬会社の責務は、疾患に対し有効な製剤を発売して終わりではありません。発売後も薬が適正に使用されているか、副作用はないか、副作用の原因は何なのか、どうしたら最も有効で安全に薬を使用してもらえるかといった安全性に関する施策を行うのが務めであり、それを担うのがファーマコビジランス職になります。
ファーマコビジランスは発売後に限らず、医薬品の開発段階から安全性に関する対策やリスクの摘出、評価を行うのが仕事であり、医薬品の適正使用と安全性・有効性の確立に努める製薬会社にとって非常に重要な機能です。
ファーマコビジランスの仕事内容

では、ファーマコビジランス職(以降PV)とは実際にどんな仕事を行うのでしょうか?
先に述べたように、PVの主な職責は「医薬品の適正使用」と「安全性対策」です。
限られた被験者に投薬する治験では安全性に問題がなかったとしても、発売後はさまざまな患者さんが薬を手にするため、治験では把握できなかった新たな症状や副作用が現れることがあります。
そのためPV担当者は、医療機関等から副作用や有害事象の情報を入手し、それらが何に起因するものなのか、重篤性などを医学的・薬学的に分析・評価したあと、問題があれば安全性対策を講じるとともに、厚生労働省に報告したり医療機関に共有したりします。
製薬会社によって、PV部が開発品・市販後製品両方の安全性業務を担当する場合と、PV部が市販後製品を担当し、開発部が開発中の薬剤の安全性を担当する場合があります。
下記のように、PVには主に2つの仕事内容があります。
医薬品の安全性監視活動
リスクマネジメント活動
①医薬品の安全性監視活動:
PVが行う医薬品の安全性監視活動には、ケースプロセッシングと呼ばれる安全性情報の収集と評価、規制当局への報告という業務があります。
治験薬や、対象試験の薬剤として使われている市販品に関する安全性情報(副作用や有害事象)を、国内の医療機関やMedWatch(米国食品医薬品局の安全性情報・有害事象報告プログラム)、FAERS(FDAの有害事象報告システム)などの海外データベースから取り寄せて収集します。
収集後は、各国の言語でさまざまに記載されている症状をMedDRA(約20万種類の用語が載っている国際医薬用語集)を使って比較分析を行い、副作用や有害事象の重篤レベルや発生頻度などによってそれらを評価していきます。選定や評価には高度な医療的知識を要するため、PV部に所属する医師が最終確認をすることが一般的です。
評価後、PMDA(独立行政法人 医薬品医療機器総合機構)への報告が必要な事象についてはCIOMSフォームなどを使用してデータベースに入力して報告が完了します。
②リスクマネジメント活動:
特定されたリスクや潜在的なリスクに対し、そのリスクを最小化するための安全対策の立案や実施を行うリスクマネジメント活動もPVの仕事です。
開発中の医薬品:治験中に得られた安全性情報や有害事象の情報をもとに、薬剤の使用中に起こりうるリスクを想定します。そのリスク要因をできるだけ排除したリスク管理計画を作成して、随時各資料に盛り込むことで安全に治験が行えるようにサポートします。具体的には、治験薬概要書の作成・改定、治験実施計画書や同意説明文書の作成・改定、PMDAと協議しながらの医薬品リスク管理計画(RMP)の作成などが挙げられます。
市販品:製造後販売調査(PMS: Post Marketing Serveillance)によって得られた情報をもとに、医師と協議しながら適宜添付文書の改訂を行います。使用条件や副作用のリスクなどが変更されるため、医療機関への周知もあわせて行います。医療従事者・患者向けの情報提供資材の作成、電子添文の改訂とお知らせ文書の作成などを行い、適正使用に向けた情報提供活動を行います。
また、PV部に製造販売後調査(PMS)の担当者を設けている企業が多くあります。
市販された医薬品は発売後4年~10年間、実際の使用現場において安全性・有効性をモニタリングし、データを収集することが義務付けられています。発売後薬剤が多くの人にどのように影響したのかを収集・分析し、より精度の高い安全性情報から新たな副作用情報やより有効性・安全性の高い用法・容量を見つけるため、GPSP(Good Post-marketing Study Practice)という調査・試験基準に基づき再審査・再評価を行います。
PMSモニターと呼ばれる職種の人たちは、こうした調査のうち使用成績調査や特定使用成績調査を担当するほか、GVP(Good Vigillance Practice)という安全管理基準に基づいて新薬発売後6か月間行われる市販直後調査についても担当しています。
ファーマコビジランスの就職先
PVの仕事に携わる場合、就職先は製薬メーカーかCRO(Contract Research Organization=医薬品開発業務受託機関)が一般的です。
CROは製薬メーカーから委託を受けて、PMSモニタリングをはじめPVに関するさまざまな業務を代行します。そのためメーカー勤務の場合、CROの担当者との連携や業務管理も職務になります。
市販後製品の安全性情報の収集は、コールセンターや調査票など複数の入手経路がありますが、各クリニックや病院の診療科を担当するMR(医薬情報担当者)と連携して収集することが多くあります。医療機関に直接聞き取りを行ったり情報共有することもあり、分析・評価した情報は厚生労働省に報告されるため、当局との協議も必要となってきます。
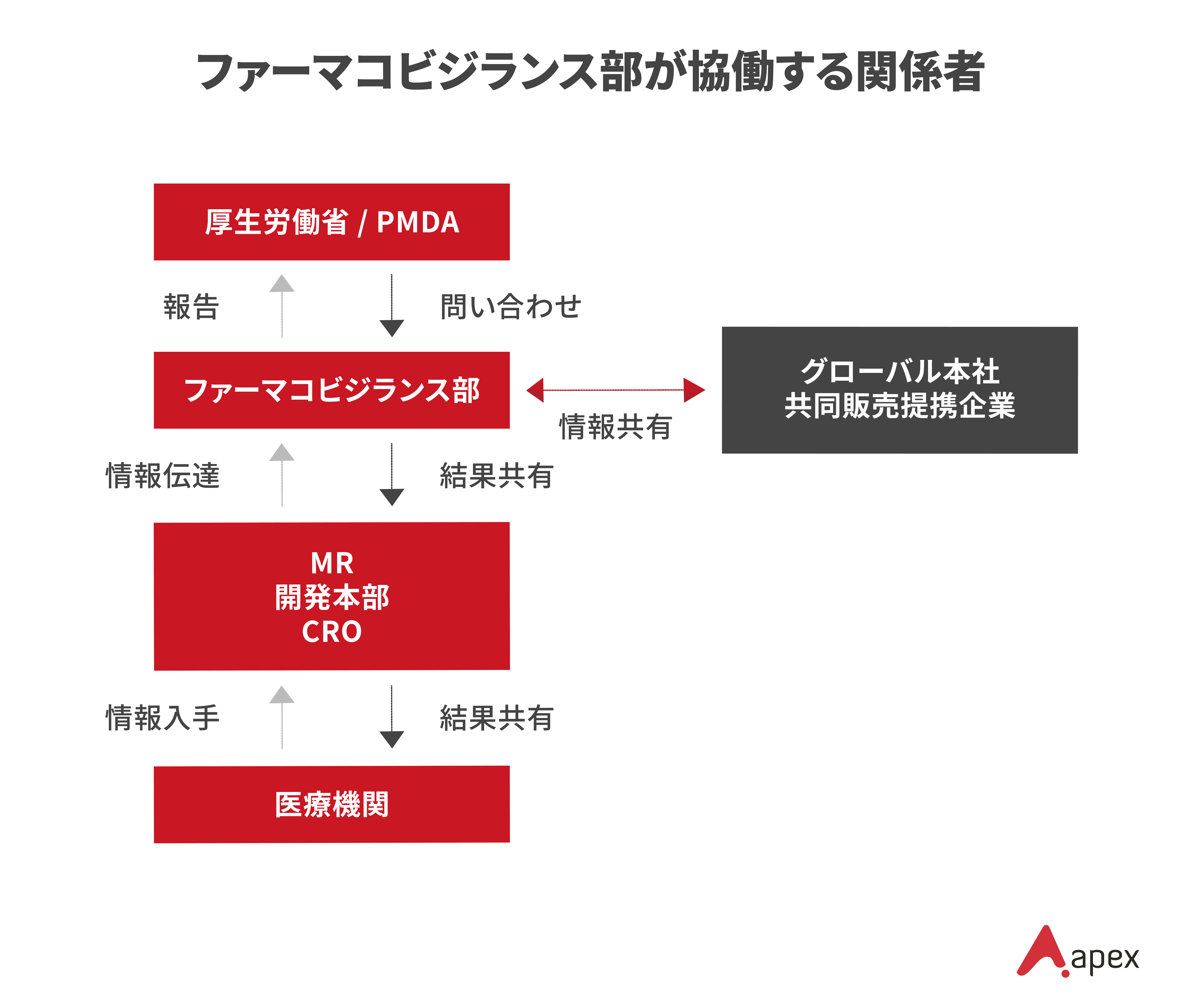
また、医薬品は日本国内だけで製造・販売されることはないため、グローバル本社や各国の担当者、アライアンスを組む他の製薬会社との連携も職務となります。開発中の製品であれば開発チームとの協業が必要であり、このようにPVは多くの関係者との協働が必要なポジションであることがわかります。
ファーマコビジランスの一日のスケジュール

では、製薬メーカーやCROのPV部で仕事をする場合、どんな働き方が一般的なのでしょうか?出張は多いのか、激務なのか、下記の一般的なPV担当者の一日のスケジュールを参考にしてみましょう。
9:00 出社、メールチェック、スケジュールチェック
9:15 チームミーティング
10:15 データベースを使った安全性情報の分析
12:00 昼休み
13:00 社内メディカルドクターとの打ち合わせ
13:30 治験実施計画書や治験薬概要書の改訂検討ミーティング
15:00 打ち合わせをもとに資料作成
17:00 安全性情報の分析
18:00 退社
このように、PVの仕事は臨機応変にさまざまな問題に対応するというよりは、データ分析や決められたフォーマットにデータを入力するなどのルーチンワークがメインとなります。通常であれば突発的な業務が発生することはあまりないので、激務ということはなく残業せずに過ごせる日が多いでしょう。ワークライフバランスが比較的整っている環境といえます。
ただ、海外のPV部門とのミーティングがある場合には、時差の関係で早朝や夜間にミーティングが入ることもあり得ます。 医療機関や関係当局に出向くことも稀にありますが、チームミーティングはリモートで行うことが多いため、スキルがあれば在宅で仕事をすることも可能です。
在宅勤務の日数は会社によって規定が異なりますので、詳細は転職エージェントに尋ねると良いでしょう。ほとんどの企業は在宅勤務とオフィス勤務のハイブリッド勤務制度を導入していますが、企業によってはフルリモートワークが可能なPVのポジションもあります。
ファーマコビジランスに求められるスキル・資格
次に、PV担当者に求められるスキルや経験を見ていきましょう。すべてに当てはまる必要はありませんが、自身がPV職に求められている特徴を持っているのか、下記を読んで確認してみましょう。
医学や薬学に関する知識・学位:安全性情報の分析や、医師とのディスカッションが可能な医学や薬学に関する知識が求められます。
専門的な論文を読んでデータ分析に役立てることもあり、医学、薬学、ライフサイエンス系の学位を取得していることが理想です。医療系資格取得者(薬剤師、看護師、臨床検査技師など)や、製薬業界従事者(MR含む)も歓迎されます。専門的な論文が読めるなどのスキルがある場合には、文系大学卒業でも転職は可能です。英語力:海外文献の読解、海外担当者とのミーティングやメールのやり取りなどが発生するため、英語スキルは必須です。特に外資系企業であれば、交渉や相談なども英語で行うことが多いため、より高度な英語力が求められるでしょう。
募集要件で提示されているTOEICの点数は600~750点以上が多く、TOEICの点数で給与が決まるところもあります。日常会話に支障がないTOEIC700点相当が求められることが多いですが、マネージャー以上のポジションになるとさらに高いレベルが必要となってきます。コミュニケーションスキル:PMDAや開発部門、CRO担当者など、PVはさまざまな部門や企業とのコミュニケーションが欠かせません。専門的な知識を部門外の人に伝えたり、より高度な知識を持つ人とディスカッションしたりすることも必要です。自分の伝えたいことを的確に伝えられる、建設的な会話ができるなどのコミュニケーションスキルが求められるでしょう。
論理的思考力:PVは毎日大量のデータを扱うため、データに基づいた論理的な思考力が必要です。さまざまなデータを使用して副作用や有害事象のレベルを決定する、英語文献を理解しながら各症例を選定していくなどのスキルが求められます。特に医師とのミーティングでは、素早く結論を出すこと、論理的に話すことが重要でしょう。
対応力:薬機法やGVP省令など医薬品関連法規は改正が多いため、フォーマットの入力方法が変わることも少なくありません。常に最新情報を確認し、自分の知識をアップデートして対応するスキルが求められます。基本的な業務はルーチンワークですが、改訂があると変化の多い対応が必要です。
ファーマコビジランスは未経験でも可能か?

製薬企業の仕事のなかでも、PVは未経験でもチャレンジできる職種の一つです。
特に、「薬剤師や看護師として実務経験があるが、企業での就業は未経験者」という方にもチャンスがある職種です。MRやCRA(臨床開発モニター)を含め、すでに製薬企業に勤めている方であれば、日常会話以上の英語スキルを持っている場合にはPVに異動することも十分可能です。
新卒入社やPV未経験で異動した際には、安全性情報の分析やDSUR(治験安全性最新報告書)作成、医療従事者やMRからの問い合わせ(メール・電話)に対応するコールセンター業務などのジュニアレベルのポジションからスタートすることが多いでしょう。
また、製薬メーカーよりもCROのほうが未経験者の中途採用に積極的です。近年は多くの製薬会社・バイオテクノロジー会社がPV業務をCROに委託しており、CROでのPV職の求人募集は数が多く、製薬会社よりも未経験者に対し柔軟です。CROでPV業務の経験を積んでから製薬会社に転職する方も多く、キャリアの入口としてCROを検討しても良いでしょう。
ファーマコビジランスの平均年収
製薬業界は、他に比べて高年収が狙える業界です。企業規模や業務範囲によって年収にばらつきはありますが、以下は製薬企業でのPV職の平均的な年収です。
部門ヘッドレベル:2,000万円前後~
マネージャーレベル(部下マネジメントあり管理職):1,200万円~1,600万円
マネージャーレベル(部下なし管理職):1,000万円~1,400万円
シニアスタッフレベル:500万円~1,100万円
ジュニアスタッフレベル:400万円~800万円
エイペックスでも、多くの方がPV職としての転職を成功され、現状よりも高い年収やポジションに就いて活躍されています。各企業の採用動向や年収レンジについてコンサルタントに詳しく聞くことができますので、ぜひ下記からキャリア面談にお申し込みください。
ファーマコビジランスが把握しておきたい業界トレンド
製薬業界では近年、安全性監視への重要性が高まっています。
特に、
希少疾患領域の医薬品の増加により、副作用の報告件数が増加傾向にあること
以前から検討されていた早期承認申請制度がコロナ禍をきっかけに正式に施工されたこと
分散型臨床試験などのデジタル技術を利用した治験が実施されるようになったこと
市販後のデータ収集の重要性の高まりから市販後大規模臨床試験が増加傾向にあること
などの点から安全性への懸念がより一層高まっており、より正確で効率的な安全性対策の必要性が論じられています。
これらのトレンドに共通していえることは、「大量の」データを「効率的に」分析・管理する高いスキルがPVに求められているということです。今後は、医療機関や消費者から集めた副作用や有害事象のデータを、PVがいかに素早くかつ正確に分析できるかという点が、薬剤の安全な使用方法の確立に大いに影響を及ぼしていくでしょう。
効率性と正確性の追及のためにはデジタル化は必須であり、PVの領域も例外ではありません。ウェアラブルデバイスを使った治験が実施されるようになったことをきっかけに、スナップデータ(ある時点における状態のデータ)からリアルタイムで更新され続ける連続データへと安全性情報も移行してきています。そのため、従来のデータ分析方法では追い付かず、今後はRPA(Robotic Process Automation)やAI技術などを積極的に活用した方法へのアップデートが求められるでしょう。
デジタル化の推進により、製薬企業はPVをはじめとしたさまざまな領域でコスト削減や業務効率化を図っており、そのため多くの企業でテクノロジーへの投資が拡大しています。PV担当者には、常に更新される業務環境に適応できる対応力が求められています。
ファーマコビジランスに関するよくある質問(Q&A)

Q. PVの求人に応募する場合、どんな志望動機がアピールにつながりますか?
A. まず、PVは英語スキルが欠かせないため、TOEICの点数やスピーキングスキルなどがある方は積極的に伝えることが大切です。英語以外にも中国語のスキルが求められる場合もありますので、能力がある方はアピールすると良いでしょう。
また、複数のプロジェクトを同時進行できるマルチタススキルやスケジュール管理能力など、優れた自己管理能力があることをアピールしましょう。ルーチンワークが多い職種のため、淡々と業務をこなすだけでなく常に改善意識を持ち、課題を設定したり論理的に解決できる能力も評価されるポイントです。
「なぜPVなのか」という答えとして、やりがいを持って業務に従事できることを伝えるのも有効です。ひとつのデータの背景にたくさんの患者さんがいる、未来の患者さんの安全性があるということを忘れずに仕事をしていけるということを、自分の言葉で語れると良いアピールにつながるでしょう。
Q. PVで経験を積んだあと、他部署に異動することは可能ですか?
A. 製薬企業やCROに就職してPVの経験を積んだあと、他のキャリアを探す方もいらっしゃいます。
PVでの業務で治験に関する知識を十分身につけていれば、難易度の違いはあれど他部署への異動は可能です。ただ、CRA(臨床開発モニター)などPVよりもコミュニケーション能力が求められる職業への異動であれば、意欲の高さや適性などが求められます。自分の希望だけでは通らないこともありますので、異動したい部署で求められるスキルをしっかりとリサーチし、スキルを磨いておくようにしましょう。
※製薬業界の品質保証(QA)の仕事内容についてはこちらの記事から
※製薬業界のMSL(メディカル・サイエンス・リエゾン)の仕事内容についてはこちらの記事から
ファーマコビジランスへの転職を成功させるために
PVに限らず、製薬業界といった特定の領域での転職を成功させるためには、情報収集とそれに基づいた戦略的な転職活動が欠かせません。
まずは、製薬業界に精通したエイペックスの人材コンサルタントとのキャリア相談会にお越しください。実績豊富なコンサルタントが、あなたの適性や希望条件をふまえ理想的なキャリアプランをご案内します。今すぐの転職ではなくても、自身の市場価値の把握や今後のための情報収集でも大歓迎です! ご興味のある方は、下記のボタンよりお申し込みください。






